Dit artikel verscheen in de 2e editie van National Geographic Magazine 2021
Stel je eens een wereld voor zonder virussen.
Zwaai met een toverstaf en doe de grote verdwijntruc. Weg is het rabiësvirus. En het poliovirus. Ook het dodelijke ebolavirus is verdwenen. Net als het mazelenvirus, het bofvirus en alle griepvirussen. In één keer zijn we verlost van een heleboel dood en verderf. Hiv bestaat niet meer – de hele aidsramp heeft nooit plaatsgevonden. We toveren ook het denguevirus weg, dat knokkelkoorts veroorzaakt. Niemand krijgt meer waterpokken, hepatitis, gordelroos of zelfs maar een verkoudheidje. Variola, het pokkenvirus? Dat was in 1977 al uitgebannen, maar nu zit het zelfs niet langer opgeborgen in de zwaarbeveiligde vriezers waar de laatste enge virusmonsters werden bewaard. Weg is het SARS-virus dat uitbrak in 2003 en achteraf een voorbode blijkt te zijn geweest van de huidige pandemie. En weg is ten slotte ook dat verdraaide SARS-CoV-2, de veroorzaker van COVID-19. Een hele verbetering, toch?
Dit scenario heeft echt niet alleen maar voordelen. Want onze wereld hangt van virussen aan elkaar – virussen in onvoorstelbaar veel variaties en in onnoemelijke aantallen. Alleen al de oceanen bevatten misschien wel meer virusdeeltjes dan er sterren zijn in het heelal. Sommige zoogdieren dragen meer dan 320.000 verschillende virussen bij zich. Tel alle virussen van de overige dieren, planten, bacteriën en andere mogelijke gastheren bij elkaar op, en je komt uit op… nou ja, véél. Die enorme aantallen hebben grote gevolgen. Veel van die virussen zijn namelijk niet alleen schadelijk, maar hebben evolutionair nut voor het leven op aarde, met inbegrip van de mens.
We kunnen ze simpelweg niet missen. Zonder virussen waren we nooit uit de oersoep tevoorschijn gekropen. En zonder de twee stukjes viraal DNA die zich door evolutie in het genoom van de mens en andere zoogdieren hebben genesteld, zou de zwangerschap – ongelooflijk maar waar – onmogelijk zijn. In het genenpakket van landdieren zit viraal DNA dat helpt om – óók al zo verbluffend – herinneringen in eiwitbolletjes te verpakken
en te bewaren. Weer andere genen van virale oorsprong bevorderen de groei van embryo’s, reguleren het immuunsysteem en beschermen ons lichaam tegen kanker – essentiële processen waarvan het bestaan pas net is aangetoond. Virussen blijken een cruciale rol te hebben gespeeld bij belangrijke evolutionaire veranderingen. Als je alle virussen wegtovert, zoals in ons gedachte-experiment, zou de immense biologische diversiteit op aarde ineenstorten als een houten huis waar je in één keer alle spijkers uittrekt.
Een virus mag dan een parasiet zijn, maar soms is dat parasitisme eerder een symbiose: een samenlevingsvorm waarbij zowel de gast als de gastheer baat heeft. Net zoals vuur zijn virussen een verschijnsel dat niet alleen kwaad brengt; ze kunnen ons slopen, maar ook vooruit helpen. Het hangt er maar net van af wat voor soort virus het is, hoe de omstandigheden zijn en vanuit welk perspectief je ernaar kijkt. Virussen zijn de duistere engelen van de evolutie, geweldig én gewelddadig. Dat is nu net wat ze zo interessant maakt.
Om virussen in al hun veelzijdigheid te waarderen, moet je eerst begrijpen wat een virus wel en niet is. Dat laatste is nog het gemakkelijkst te bepalen. Een virus is namelijk geen levende cel. Een cel, waarvan ieder mens – maar bijvoorbeeld ook een octopus of een netelbloem – er miljarden bezit, bevat een ingenieus mechanisme voor de aanmaak van eiwitten, de opslag van energie en het uitvoeren van andere taken. Zo is een bacterie ook een cel, met vergelijkbare eigenschappen, maar dan veel eenvoudiger. Een virus is dat dus allemaal niet.
Uitleggen wat een virus dan wél is, is zo ingewikkeld dat de definities de afgelopen 120 jaar nogal eens zijn veranderd. De Nederlandse botanicus en microbioloog Martinus Beijerinck, die onderzoek deed naar het tabaksmozaïekvirus, opperde in 1898 dat het wellicht een besmettelijke vloeistof was. Vervolgens werd een virus gedefinieerd aan de hand van zijn omvang: het was een ziektekiem die een stuk kleiner was dan een bacterie maar, net als een bacterie, een ziekte kon veroorzaken. Later werd een virus gezien als een submicroscopisch organisme met een minuscuul genoom dat zich in levende cellen vermenigvuldigde – een eerste stap in de juiste richting.
‘Ik ga een paradoxaal standpunt verdedigen,’ schreef de Franse microbioloog André Lwoff in 1957 in zijn invloedrijke essay The Concept of Virus, ‘namelijk dat virussen virussen zijn.’ Zo op het oog niet bepaald een baanbrekende nieuwe definitie, maar wel een opmaat tot de opvatting dat ze ‘volkomen uniek’ zijn.
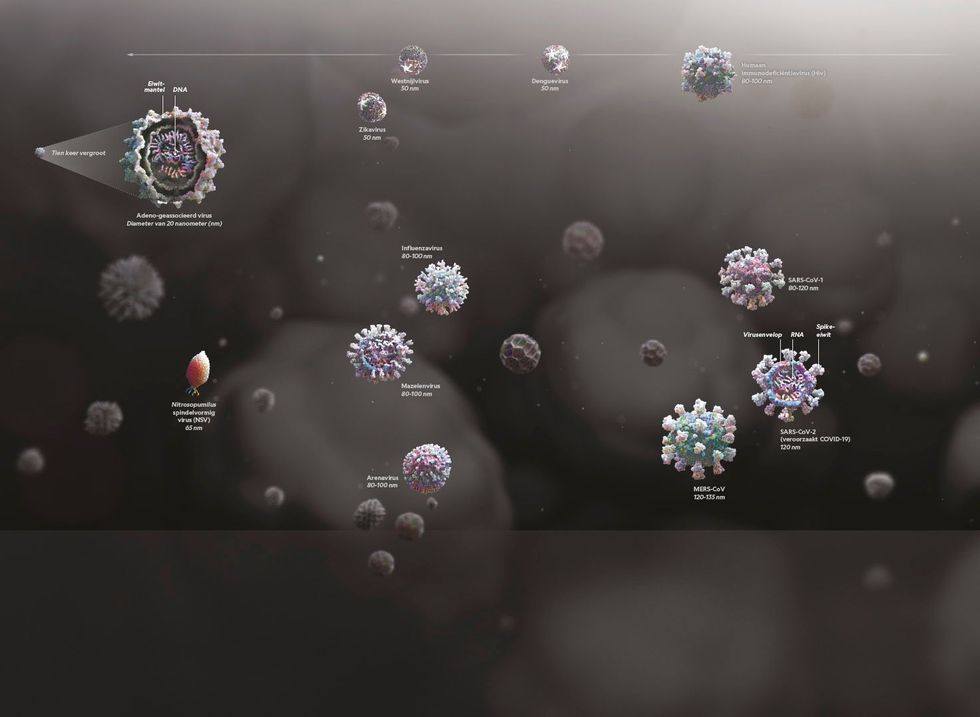
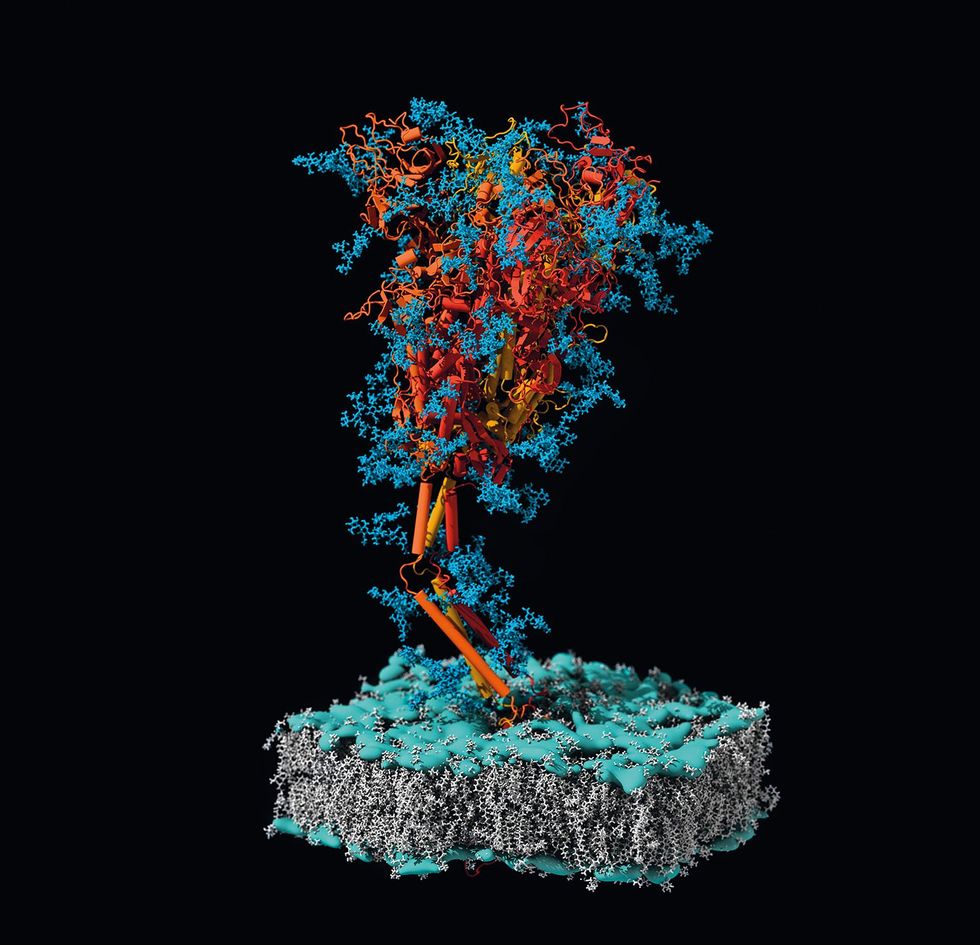
Lwoff zag in dat virussen zich eenvoudiger laten beschrijven dan definiëren. Elk virusdeeltje bestaat uit een sliert genetische instructies (geschreven in DNA of in dat andere informatiedragende molecuul, RNA) verpakt in een eiwitmantel (ook wel capside genoemd). Soms zit er rondom die eiwitmantel nog een membraan (of envelop) dat ter bescherming dient en het virus helpt om een cel vast te grijpen. Een virus kan zichzelf alleen vermenigvuldigen door een cel binnen te dringen en diens 3D-printer te hacken die genetische informatie omzet in eiwitten.
Als de gastheer pech heeft, worden er vervolgens zo veel nieuwe virusdeeltjes geproduceerd dat ze naar buiten barsten en de cel als een wrak achterlaten. Door dat soort schade, zoals SARSCoV-2 aanricht in de epitheelcellen van onze luchtwegen, kan een besmet persoon flink ziek worden.
Maar als de gastheer boft, kruipt het virus in dat knusse holletje om er rustig te gaan slapen of er zijn genoom te installeren. In dat laatste geval wordt er genetische informatie uitgewisseld, en dat heeft gevolgen voor onze evolutie en zelfs voor ons idee van wat we zijn, maar daarover later meer. Toch alvast een tipje van de sluier. In een populair boek uit 1983 stelden de Britse bioloog Peter Medawar en zijn vrouw Jean: ‘Er is geen enkel virus bekend dat iets goeds doet. Het is weleens treffend omschreven als ‘een brokje slecht nieuws verpakt in eiwit’.’ Ze zaten er faliekant naast, net als veel andere wetenschappers uit die tijd. En logischerwijs leeft dat idee nog steeds bij mensen die virussen alleen kennen van slecht nieuws als griep en COVID-19. Maar inmiddels weten we beter en kennen we ook virussen die wel degelijk iets goeds doen. In de eiwitverpakking zit een genetisch telegram, met slecht óf goed nieuws.
Hoe zijn de eerste virussen ontstaan? Daarvoor moeten we bijna vier miljard jaar terug in de tijd, toen de aarde nog een primitieve stoofpot was van lange moleculen, simpele organische verbindingen en energie.
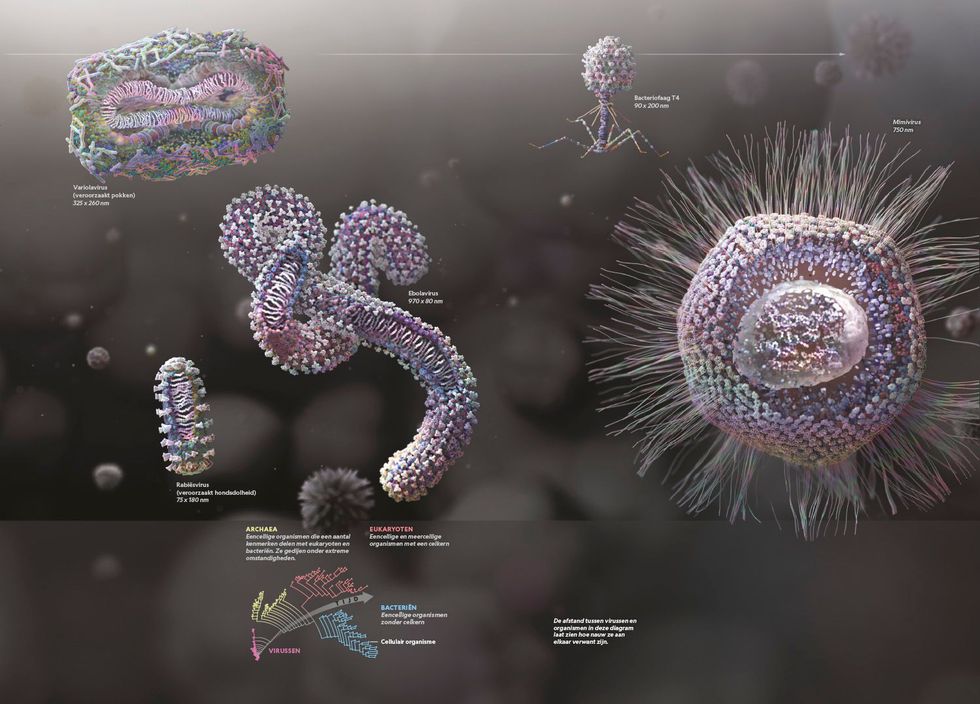
Laten we aannemen dat een deel van die lange moleculen (waarschijnlijk RNA) zich is gaan reproduceren. Toen moet Darwins natuurlijke selectie zijn begonnen, doordat die moleculen – de eerste genenklompjes – tijdens dat proces muteerden en evolueerden. Sommige moleculen kregen wellicht een voorsprong op andere door bescherming te vinden in membranen en wanden, waardoor de eerste cellen ontstonden. Die cellen vermenigvuldigden zich door zich in tweeën te splitsen. Maar ze splitsten zich ook in bredere zin: ze vertakten zich tot bacteriën en archaea, twee van de drie domeinen van cellulair leven. Het derde domein, de eukaryoten, zou pas later ontstaan; dat omvat ons en alle andere schepselen (dieren, planten, schimmels, bepaalde microben) die zijn opgebouwd uit cellen met een complexe inwendige anatomie. Bacteriën, archaea en eukaryoten zijn de drie grote takken aan de boom des levens zoals die wordt beschreven volgens de huidige stand van de wetenschap.
Maar welke rol spelen virussen in dit geheel? Vormen ze een vierde grote tak? Meestal worden de virussen gemakshalve weggelaten uit de levensboom. Volgens sommige wetenschappers horen virussen er niet thuis omdat het geen levende organismen zouden zijn. Dat is geen al te sterk argument, want het hangt er maar net van af hoe je ‘levend’ definieert. Het is interessanter om virussen een plek te gunnen in de grote tent van het leven en je vervolgens af te vragen hoe ze naar binnen zijn geglipt.
De drie belangrijkste hypothesen om de evolutionaire oorsprong van virussen te verklaren, worden in wetenschappelijk jargon de ‘virus eerst’-hypothese, de ontsnappingshypothese en de reductiehypothese genoemd. De eerste hypothese gaat ervan uit dat virussen eerder bestonden dan cellen en op de een of andere manier rechtstreeks uit de oersoep zijn ontstaan. Volgens de ontsnappingshypothese maakten genen of stukjes genoom zich juist los uit cellen, trokken ze een jasje van eiwit aan en begonnen ze voor zichzelf. De reductiehypothese stelt dat virussen hun oorsprong vinden in cellen die almaar compacter werden en steeds meer genen afstootten, totdat ze zo uitgekleed waren dat ze alleen nog konden voortbestaan door op andere cellen te parasiteren.
Er is nog een vierde variant, de chimerische hypothese, met in de hoofdrol een andere categorie genetische elementen: transposons, ook wel springende genen genoemd. Deze opportunisten danken hun evolutionaire succes aan hun vermogen om van het ene deel van een genoom naar het andere over te springen, van de ene cel naar de andere, of zelfs van de ene planten- of diersoort naar de andere, waarbij ze cellen benutten om zichzelf steeds opnieuw te kopiëren. Dankzij die eindeloze reproductie lopen ze geen risico uit te sterven. Ze vermeerderen zich zelfs zo enthousiast dat ze pakweg de helft van het menselijk genoom uitmaken. Op basis van deze hypothese zijn de eerste virussen ontstaan doordat zulke elementjes eiwitten van cellen leenden om zich in een beschermende mantel te hullen.
Voor al deze hypothesen valt iets te zeggen. Maar in 2003 werd een ontdekking gedaan die het wetenschappelijk debat leek te beslechten in het voordeel van reductie: het reuzenvirus.
Het reuzenvirus werd gevonden in amoeben, eencellige eukaryoten. Die amoeben, uit een koeltoren in het Engelse Bradford, bleken een mysterieus klontje te herbergen. Dat was zo groot dat het zichtbaar was onder een lichtmicroscoop (tot dan toe dacht men dat virussen zo klein waren dat ze alleen te zien waren met een elektronenmicroscoop), en het leek nog het meest op een bacterie. Maar onderzoekers zochten vergeefs naar bacteriële genen. Uiteindelijk werd het raadsel opgelost door een onderzoeksteam in Marseille. Ze lieten het klontje nog meer amoeben besmetten, brachten het genoom in kaart, ontdekten wat het was en doopten het mimivirus, een afkorting van mimicking microbe, omdat het een bacterie leek na te bootsen. Het had een reusachtige diameter voor een virus, groter dan die van een kleine bacterie. Ook het genoom was kolossaal: bijna 1,2 miljoen letters lang, terwijl het pokkenvirus er maar 194.000 telt en het griepvirus 13.000. (DNA is net als RNA een lang molecuul dat is opgebouwd uit vier verschillende moleculaire basen die worden genoemd naar hun beginletter.) Het was een virus dat eigenlijk niet kon bestaan: het had de eigenschappen van een virus, maar was veel te groot – alsof er in de Amazone een nieuwe vlinder zou worden ontdekt met een spanwijdte van een meter.
Een van de onderzoekers van het Zuid-Franse team was Jean-Michel Claverie. De ontdekking van het mimivirus was ‘nogal problematisch’, vertelt hij. Bij het in kaart brengen van het genoom doken namelijk vier genen op die niet in het plaatje pasten – genen voor het coderen van enzymen, waarvan men dacht dat ze alleen in cellen voorkwamen en die nooit eerder bij een virus waren gezien. Die enzymen, legt Claverie uit, spelen een rol bij het samenklonteren van aminozuren tot eiwitten. ‘De vraag was dus,’ stelt Claverie, ‘wat een virus in hemelsnaam aan moest met de luxe van enzymen’, die normaal gesproken alleen actief zijn in cellen, ‘terwijl het gewoon een cel tot zijn beschikking heeft.’
Een verklaring die hout snijdt, is dat de enzymen restanten zouden zijn van een cel waaruit het mimivirus ooit is ontstaan door genetische reductie.
De ontdekking stond niet op zichzelf. Algauw werden er ook reuzenvirussen aangetroffen in de Sargassozee en werd de naam mimivirus gebruikt als soortnaam voor een hele reeks giganten. Het Franse onderzoeksteam vond er zelf ook nog twee: een in een sliblaag voor de kust van Chili en een in een meertje in Australië. Deze exemplaren waren tot twee keer zo groot als het eerste mimivirus en verschilden ook in andere opzichten zo sterk dat ze werden bestempeld als een aparte soort, die Claverie en zijn collega’s het pandoravirus noemden – naar de doos van Pandora, omdat ze erop rekenden dat ze ‘bij vervolgonderzoek op nog veel meer verrassingen zouden stuiten’.
Claverie publiceerde zijn resultaten samen met zijn vrouw, viroloog en structuurbioloog Chantal Abergel. Met een vermoeid lachje zegt Abergel nu over de pandoravirussen: ‘Ik had er mijn handen aan vol. Het zijn echt mijn kindjes.’ Ze vertelt hoe moeilijk het was om erachter te komen wat deze wezentjes waren. Ze leken niet op cellen, ze leken niet op klassieke virussen, en ze hadden allerlei genen die niemand ooit eerder had gezien. Aanvankelijk dacht ze op een nieuwe levensvorm te zijn gestuit, maar toen bleek dat de organismen zich niet door deling vermeerderden, begrepen Abergel en haar collega’s dat ze met virussen te maken hadden – de grootste en bizarste die er tot dusver waren ontdekt.
Zo kwam het onderzoeksteam op een gewaagde variant op de reductiehypothese. Misschien waren virussen inderdaad oeroude cellen, maar dan ontstaan uit cellen die nu niet meer op aarde voorkomen. Die ‘voorouderlijke protocellen’ verschilden van de universele voorloper van alle cellen die we vandaag de dag kennen. Misschien hebben ze ermee gewedijverd en de strijd verloren, en zijn ze vervolgens verdreven uit alle plekken waar zelfstandig levende schepsels terechtkonden. Wellicht hebben ze zich gered door te parasiteren op andere cellen, zich te ontdoen van een deel van hun genoom en te veranderen in wat we nu virussen noemen. In dat geval zouden virussen de enige overblijfselen zijn uit dat verdwenen cellenrijk.
De ontdekking van reuzenvirussen bracht andere wetenschappers, onder wie Patrick Forterre van het Institut Pasteur in Parijs, op nieuwe ideeën over wat virussen nou eigenlijk zijn en wat hun functie is.
Eerdere definities van virussen voldeden niet, zegt Forterre, omdat wetenschappers virusdeeltjes – de plukjes erfelijk materiaal in hun eiwitjasje, officieel virionen geheten – verwarden met virussen als geheel. Dat is volgens hem net zoiets als een zaadje met een plant verwarren. Het virion is niet meer dan het verspreidingsmechanisme, stelt hij. Het virus als geheel omvat ook zijn aanwezigheid in een geïnfecteerde cel, waarvan hij de machinerie gebruikt om meer virionen te maken, meer kopieën van zichzelf. Kijk je naar beide verschijningsvormen, dan zie je dat het virus de cel deel heeft gemaakt van zijn levensgeschiedenis.
Om zijn idee kracht bij te zetten, lanceerde Forterre een nieuwe naam voor de twee-eenheid: virocel. Het gaf meteen antwoord op het levend-of-niet-vraagstuk. Een virus leeft als het een virocel is, stelt hij, ook al leven de virionen zelf niet.
‘De gedachte achter het concept van de virocel,’ vertelt Forterre via Skype vanuit Parijs, ‘was om vooral naar het intracellulaire stadium te kijken.’ Dat is de precaire fase waarin de geïnfecteerde cel als een zombie de virale bevelen opvolgt, het virale genoom uitleest en kopieert, maar daarbij soms struikelt, stukjes overslaat en fouten maakt. Tijdens dat proces, zegt Forterre, ‘kunnen er nieuwe genen in het virale genoom terechtkomen. Dat is voor mij een essentieel punt.’ Virussen brengen vernieuwing, maar cellen komen in reactie daarop met vernieuwingen ter verdediging, zoals de celwand of de celkern, waardoor er een wapenwedloop ontstaat die leidt tot een steeds grotere complexiteit.
Volgens veel wetenschappers evolueren virussen door ‘zakkenrollerspraktijken’: ze pikken DNA uit de organismen die ze infecteren en gebruiken de buit in hun eigen genoom. Maar volgens Forterre is het vaker net andersom en nemen cellen juist genen van virussen over.
Nog een stap verder gaat de opvatting van Forterre, Claverie en anderen dat virussen de belangrijkste aanjager zijn van genetische diversiteit. Virussen, stellen ze, hebben in de voorbije miljarden jaren de evolutionaire mogelijkheden van cellulaire organismen vergroot door voortdurend nieuw erfelijk materiaal in hun genomen te brengen. Dat bizarre proces is een vorm van zogeheten horizontale genoverdracht, de uitwisseling van genen tussen twee organismen zonder familieverwantschap. (Bekender is de verticale vorm van genoverdracht, van ouders aan hun nakomelingen.) Er is ‘overweldigend’ veel genetisch materiaal van virussen overgegaan naar dat van cellen, schreef Forterre met een medeauteur, en dat heeft een rol gespeeld bij bepaalde grote sprongen in de evolutie, zoals het ontstaan van DNA, het ontstaan van de celkern in complexe wezens, het ontstaan van de celwanden, en misschien zelfs het uiteengroeien van de drie grote levensdomeinen.
Vroeger, vóór COVID-19, sprak ik wetenschappers nog weleens uitvoerig in levenden lijve in plaats van via Skype. Zo vloog ik drie jaar geleden van Montana (VS) naar Parijs om een man uit te horen over een virus en een gen. De man in kwestie was Thierry Heidmann, het gen syncytine-2. Heidmann was er met zijn collega’s op gestuit toen ze het complete menselijk genoom – alle 3,1 miljard letters van de code – doorspitten op zoek naar stukjes DNA die een virus zou kunnen gebruiken voor het maken van zijn envelop. Ze vonden er ongeveer twintig.
‘Zeker twee bleken erg belangrijk te zijn,’ vertelde Heidmann. En dat kwam doordat ze taken konden uitvoeren die van cruciaal belang zijn bij de menselijke zwangerschap. Die twee genen waren syncytine-1, dat al eerder was gevonden, en syncytine-2, dat hij en zijn collega’s zelf ontdekten. Hoe die virale genen in het menselijk genoom zijn gekomen en wat ze er doen, is een wonderbaarlijk verhaal dat begint met het principe van menselijke endogene retrovirussen. Een retrovirus is een virus met een RNA-genoom dat precies andersom werkt als andere virussen. In plaats van DNA te gebruiken om RNA te maken, dat vervolgens opdracht geeft aan de 3D-printer in de cel om eiwitten te produceren, laten deze virussen DNA maken door hun RNA dat ze vervolgens in het genoom stoppen van de besmette cel. Hiv is zo’n retrovirus, dat menselijke immuuncellen infecteert en zijn eigen genoom in dat van de cel verankert, waar het soms een tijd blijft sluimeren. Zodra het virale DNA wordt geactiveerd, fungeert het als sjabloon voor de massaproductie van hiv-virionen, die de cel uiteindelijk laten exploderen.
Maar nu komt het bijzondere: sommige retrovirussen dringen de geslachtscellen binnen – de cellen die eicellen of sperma aanmaken – en verankeren hun DNA in het erfelijk materiaal van de gastheer. Die nieuwe stukjes DNA zijn ‘endogene’ (lichaamseigen) retrovirussen, en eenmaal opgenomen in het menselijk genoom worden ze menselijke endogene retrovirussen (HERV’s) genoemd. Als u één ding van dit artikel moet onthouden, is het dat het menselijk genoom voor acht procent bestaat uit zulk viraal DNA, dat tijdens onze evolutie door retrovirussen ons erfelijk materiaal is binnengeloodst. En syncytine-2 is een van de belangrijkste stukjes viraal DNA dat we in ons lichaam hebben.
Urenlang heb ik bij Heidmann op zijn kamer gezeten terwijl hij me alles vertelde over de oorsprong en functies van dit ene gen. Waar het op neerkomt, is niet eens zo ingewikkeld. Een gen dat ooit een virus hielp om met cellen van de gastheer te versmelten, heeft zich lang geleden in dierlijke genomen genesteld. Daar kreeg het de nieuwe taak om een vergelijkbaar eiwit te maken dat cellen liet versmelten tot een vlies rondom hetgeen dat later de placenta zou worden, en dat dieren een nieuwe mogelijkheid bood: inwendige zwangerschap.
Het eerste retrovirale gen dat hiervoor zorgde, werd na verloop van tijd ingeruild voor vergelijkbare genen die nog beter op hun taak waren toegerust. Gaandeweg werd het ontwerp voor deze nieuwe voortplantingsmethode steeds verder vervolmaakt en functioneerde de placenta steeds beter. En dat komt onder meer door syncytine-2. Dat unieke doorgeefluik tussen moeder en kind zorgt voor de aanvoer van voedingsstoffen en zuurstof, de afvoer van afvalstoffen en kooldioxide, en beschermt het kind vermoedelijk ook tegen aanvallen door het immuunsysteem van de moeder. En dit wonder komt op het conto van een stukje virus dat zich heeft ontwikkeld tot een stukje mens.
Toen het me ten slotte begon te duizelen en ik mijn hele notitieboekje had volgeschreven, vroeg ik Heidmann wat dit hele verhaal nu zegt over de werking van de evolutie? Hij begon te lachen, en ik lachte uit beleefdheid met hem mee. ‘Dat onze genen niet alleen ónze genen zijn,’ antwoordde hij. ‘Onze genen zijn ook de genen van retrovirussen.’
De bijdrage van het retrovirus waaraan we syncytine-2 te danken hebben, is maar een schakeltje in een groter plaatje. Een ander voorbeeld is het gen ARC, dat wordt ingeschakeld door neuronale activiteit. Het lijkt sterk op een retroviraal gen dat codeert voor een bepaalde eiwitmantel. Recent onderzoek heeft aangetoond dat ARC een belangrijke rol speelt bij de opslag van informatie in neurale netwerken – anders gezegd: het geheugen. ARC doet dat waarschijnlijk door informatie uit ervaringen (vastgelegd in RNA) in kleine eitwitzakjes te verpakken die vervolgens van het ene neuron naar het andere worden getransporteerd.
Aan de Stanford University School of Medicine hebben Joanna Wysocka en haar collega’s aanwijzingen gevonden dat virale deeltjes die zijn aangemaakt door een ander menselijk endogeen retrovirus, HERV-K, al in het vroegste stadium in een embryo zitten en het jonge leven mogelijk helpen te beschermen tegen virusinfecties, een rol spelen bij de groei, of allebei. Ook heeft Wysocka’s team zich gebogen over een bepaald transposon, dat als een soort voorloper van HERV-K het menselijk genoom is binnengedrongen, zichzelf heeft gekopieerd en is overgesprongen naar andere delen van het genoom. Nu zit het in 697 her en der verspreide kopieën, die vermoedelijk bijna driehonderd menselijke genen helpen te activeren.
‘Wat ik echt ongelooflijk vind,’ zegt Wysocka, ‘is dat HERV’s zo’n acht procent uitmaken van het menselijk genoom,’ een deel van ons dat in feite ‘het kerkhof van oude retrovirale infecties’ is. Nog ongelooflijker vindt ze de gedachte dat ‘de hele geschiedenis van retrovirale infecties tot op de dag van vandaag een stempel drukt op de evolutie van onze soort’.
Het nadeel van deze evolutionaire souplesse is dat virussen naar een andere gastheer kunnen overspringen en zich daar kunnen ontpoppen als een geraffineerde ziekmaker. Dat is precies hoe de meeste nieuwe infectieziekten bij de mens ontstaan: als een mens een virus oploopt dat afkomstig is van een dier.
Bij de oorspronkelijke gastheer, in wetenschappelijk jargon een reservoir geheten, kan zo’n virus zich duizenden jaren koest hebben gehouden. Misschien heeft het een evolutionair dealtje gesloten met die gastheer om geen problemen te schoppen in ruil voor een veilig plekje. Maar bij een nieuwe gastheer, bijvoorbeeld de mens, geldt de oude afspraak niet altijd meer. Dan kan het virus zich als een malle gaan vermeerderen en zijn eerste slachtoffer flink ziek maken. Als het virus zich van mens op mens weet te verspreiden en tientallen ziektegevallen veroorzaakt, spreken we van een uitbraak. Wanneer het door een hele stad of een land raast, noemen we het een epidemie. Gaat het ten slotte de hele wereld over, dan hebben we een pandemie. En zo komen we terug bij SARS-CoV-2.
Bij sommige soorten virussen is de kans op een pandemie groter dan bij andere. Boven aan de lijst van gevaarlijkste kandidaten staan coronavirussen, door de aard van hun genoom, hun vermogen om te veranderen en te evolueren, en door de eerdere luchtwegziekten waarmee ze de mens hebben opgezadeld, zoals SARS en MERS. Dus toen er ineens over een ‘nieuw coronavirus’ werd gesproken dat besmettingen veroorzaakte in de Chinese stad Wuhan, sloeg virologen de angst om het hart.
Coronavirussen zijn enkelstrengige RNA-virussen, een beruchte categorie waartoe ook influenza, ebola, mazelen, nipah, hanta- en retrovirussen behoren. Een van de redenen achter die slechte reputatie is dat een eenstrengig RNA-genoom bij reproductie van het virus vaak muteert, en dat die mutaties voor een grote genetische variatie zorgen waar het virus via natuurlijke selectie zijn voordeel mee doet.
Toch evolueren coronavirussen voor RNA-virussen verhoudingsgewijs traag. Hun genoom is vrij groot, maar het verandert minder snel dan dat van sommige andere virussen, omdat ze een enzym bezitten dat fouten signaleert en corrigeert. Wel beheersen ze een ander gevaarlijk kunstje, dat van recombinatie, waarbij twee varianten van het coronavirus die dezelfde cel hebben besmet delen van hun genoom uitwisselen. Hierdoor ontstaat een derde, hybride virusvariant. Het nieuwe coronavirus, SARS-CoV-2, is mogelijk op die manier ontstaan. Het oorspronkelijke virus kan afkomstig zijn geweest van een vleermuis, wellicht een grote hoefijzerneus. Als het virus inderdaad is gerecombineerd met cruciale nieuwe elementen van een ander virus, dan is het best mogelijk dat dat in een vleermuis is gebeurd. Onderzoekers proberen de ‘dader’ te achterhalen door het genetisch materiaal van virussen die bij diverse potentiële gastheren zijn gevonden te analyseren en te vergelijken. Het enige dat we op dit moment zeker weten, is dat SARS-CoV-2 een flexibel virus is dat zich in de toekomst nog verder kan evolueren.
Dus virussen zijn zowel goed als slecht voor ons. Misschien is hun plek aan de levensboom wel zo lastig aan te wijzen omdat de geschiedenis van het leven in werkelijkheid niet de vorm heeft van een boom. Die botanische vergelijking is enkel de traditionele manier om de evolutie, de canonieke theorie van Charles Darwin, in beeld te brengen. Maar hoe groot hij ook was, Darwin wist niets van virussen. Als de gedachte dat we zelf voor een deel uit virussen bestaan ons uit de droom helpt dat we boven alles verheven zijn, dan laat ik het aan u over om te bepalen of dat goed of slecht voor ons is.
David Quammen heeft zestien boeken geschreven, waaronder Zoönose, waarin hij COVID-19 voorspelde. Craig Cutler legt zich als kunstenaar en fotograaf toe op stillevens en het milieu, waarbij hij in elk beeld een verhaal wil vertellen.
Dit artikel verscheen in de 2e editie van National Geographic Magazine 2021